Revista Canal Abierto 45 | Caso Clínico
Retratamiento Quirúrgico Endodóntico. Reporte de Caso.
Aceptado: 25-01-2022
Páginas 40-45
Lenin Gabriel Gárate C. 1, Alison Pamela Álvarez B.2, José Nestorio Astudillo S.3, Fernanda Katherine Sacoto-F.1
- Odontólogo Especialista en Endodoncia. Práctica privada.
- Egresado de la Carrera de Odontología. Universidad Católica de Cuenca, Ecuador.
- Odontólogo Especialista en Periodoncia e Implantologia. Práctica privada.
- Odontólogo Especialista en Endodoncia . Docente titular. Universidad Católica de Cuenca, Ecuador.
Resumen
Se presenta un caso de un diente 2.2 con periodontitis apical persistente, el mismo que por sus signos y síntomas se relaciona a un cuadro de infección extrarradicular independiente. El caso no responde favorablemente a técnicas de endodoncia ortógrada, medicación intracanal y antibioticoterapia, siendo tratado exitosamente mediante endodoncia quirúrgica. Radiográficamente muestra una zona radiolúcida difusa periapical de aproximadamente 13 mm de diámetro, obturación completa del canal radicular, apicectomía previa realizada hace 10 años. Clínicamente presenta fístula y una restauración coronal desadaptada. Este artículo describe un plan de tratamiento quirúrgico endodóntico capaz de resolver la patología, signos, síntomas ,y promover reparación del área periapical.
Pablabras clave: Apicectomía. Obturación retrógrada. Periodontitis Apical Persistente. Silicato de calcio.
Abstract
A case of a tooth 2.2 with persistent apical periodontitis is presented, which due to its signs and symptoms is related to an independent extraradicular infection. The case does not respond favorably to orthograde endodontic techniques, intracanal medication and antibiotic therapy. Being successfully treated by surgical endodontics. Radiographically, it shows a periapical diffuse radiolucent zone of approximately 13 mm in diameter, complete obturation of the root canal, previous apicoectomy performed 10 years ago. Clinically it presents a fistula, and a coronal restoration whitout marginal integrity. This article describes an endodontic surgical treatment plan capable of resolving the pathology, signs, symptoms and promoting the repair of the periapical area.
Keywords: Apicoectomy. Retrograde obturation. Apical Periodontitis. Calcium silicate.
Introdución
El fracaso del tratamiento quirúrgico endodóntico puede relacionarse al desarrollo de infección extrarradicular independiente en los tejidos perirradiculares. (1,2) En el pasado se realizaban técnicas tradicionales de preparación del espacio apical del canal radicular con una fresa redonda y usando amalgama como material de obturación retrógrada. En las últimas décadas los avances respaldados por investigaciones han llevado a un refinamiento de técnicas y materiales que definen a la cirugía apical en la actualidad, obteniendo una tasa de éxito que llega al 80%, con una resolución de síntomas, reparación apical y regeneración ósea periapical. (3-5)
El uso de magnificación, puntas de ultrasonido y cementos a base de silicato de calcio son un factor clave en el éxito de la endodoncia quirúrgica según varios autores (5,6-9), lo que permite una preparación y sellado más eficaz a lo largo del eje del canal radicular, sin bloquear la visibilidad al operador.
La decisión de tratar un caso quirúrgicamente o no es un desafío que debe basarse en las circunstancias individuales de cada caso; es una opción de tratamiento que se prefiere a la extracción o implante. El éxito del tratamiento endodóntico quirúrgico es poco abordado; esta terapia requiere un enfoque multidisciplinario que implica el manejo correcto de biocerámicos en endodoncia y regeneración ósea guiada en periodoncia. Por lo antes mencionado, se presenta un caso de cirugía periapical previa fallida, donde solamente identificando el factor causal podremos solucionar la patosis perirradicular mediante su manejo individual.
Presentación del Caso Clínico
Paciente sexo femenino de 54 años de edad acude a consulta por presencia de fistula en el sector anterior del maxilar, con 15 días de evolución. Durante la anamnesis refiere tener un tratamiento endodóntico de 15 años de antigüedad en el diente 2.2; el mismo tuvo un procedimiento quirúrgico hace 10 años. A la exploración clínica se observó una fístula que se corroboró mediante fistulografía asociada al diente 2.2. La paciente no manifiesta dolor, está asintomática a la palpación y percusión, se realizó un sondaje periodontal obteniendo 3 mm de profundidad. Radiográficamente se observa una zona radiolúcida difusa periapical, cu- briendo el área del diente 2.2, con aproximadamente 13 mm de diámetro, obturación completa del canal radicular, ápice abierto y restauración coronal desadaptada. (Fig.1)
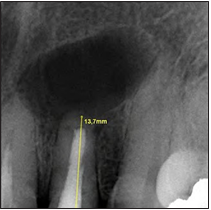
Figura 1. Radiografía periapical inicial.
El diagnóstico del diente 2.2 es diente previamente tratado y absceso apical crónico.
Se planificó el retratamiento y apicoformación para el diente. Se recomienda a la paciente considerar retratar el diente 2.1 por lo observado en la radiografía (obturación corta y deficiente), la paciente decide tratar el diente 2.2 y postergar el tratamiento del diente 2.1.
En la primera sesión del diente 2.2 se retiró la restauración defectuosa con una fresa endo access FG 2 (Dentsply Maillefer, Ballaigues, Switzerland ), se desobturó el canal radicular con una lima reciprocante Reciproc Blue R50 (VDW, Munich, Germany) y xilol (Prodont, Bogotá, Colombia) como solvente. Después de retirar el material de obturación antiguo y obtener permeabilidad, hubo drenaje profuso. Debido a las condiciones del caso, se utilizó una lima K#70 (Dentsply Maillefer, Ballaigues, Switzerland) para obtener la longitud de trabajo, obteniendo una longitud electrónica apical de 15mm, la cual se confirmó mediante conductometría. La instrumentación se realizó hasta lima K#80 (Dentsply Maillefer, Ballaigues, Switzerland). Durante la preparación quimiomecánica se irrigó de forma constante con hipoclorito de sodio al 5%.
El canal radicular dejó de drenar exudado, se realizó un protocolo de irrigación EDTA (EDTA Eufar,Bogotá,Colombia) al 17% por 1 minuto mediante activación sónica pasiva con endoactivador (Dentsply Maillefer, Ballaigues, Switzerland), seguido de 3ml de hipoclorito de sodio al 5% y activación sónica de este irrigante, realizando cambios de solución cada 20 segundos, se colocó hidróxido de calcio intracanal por 7 días (Ultracal; Ultradent, South Jordan, UT), una base de teflón como material de separación y se selló la cavidad de acceso con cemento provisional a base de óxido de zinc, Fermín (Detax, Ettlingen, Germany).
En la segunda sesión, la fístula ha cicatrizado, sin embargo al retirar el provisional y el teflón se observó un drenaje profuso vía cameral, por lo que se decidió recapitular la instrumentación e irrigación copiosa con hipoclorito de sodio al 5%. Una vez que se logró obtener un canal radicular seco, se selló nuevamente el acceso, finalizando esta segunda sesión con medicación sistémica (amoxicilina + ácido clavulánico 875mg por 5 días).
En una tercera sesión, aún se observó drenaje vía cameral. Se decidió alargar el tratamiento antibiótico sistémico hasta el día 10. En la cuarta sesión se realiza el protocolo de irrigación y se coloca medicación intracanal nuevamente por 7 días.
En la quinta sesión, el paciente aún no presenta condiciones ideales para realizar apicoformación y una obturación, por lo cual se decide realizar un abordaje quirúrgico de este caso.
Después de la asepsia y antisepsia de la zona quirúrgica, se procedió con el bloqueo del nervio alveolar superior anterior y nervio nasopalatino (lidocaína 2% con epinefrina 1:80 000 Xylestesin, 3M ESPE, GERMANY), se realizó una incisión paramarginal con una hoja de bisturí #15 y posterior elevación del colgajo de espesor total. Ya expuesta la raíz (Fig. 2), se realizó la enucleación de la lesión, limpieza del campo quirúrgico mediante una fresa redonda de carburo tungsteno y rectificación del corte apical corrigiendo el bisel anterior por un bisel de 0° (Fig. 3). Con una gasa estéril impregnada de anestésico con vaso constrictor, se aplicó para el control de la hemorragia.
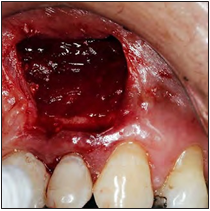
Figura 2. Primera exposición del área periapical.
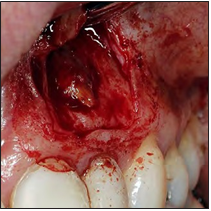
Figura 3. Apicectomía y enucleación de la lesión.
Durante las sesiones de endodoncia y para el procedimiento quirúrgico se utilizó magnificación de 4.0 x (Epic Loupes, LLC, Idaho, USA).
La caja de obturación fue conformada con una punta de ultrasonido P1M (Helse Ultrasonic, Santa Rosa do Viterbo, Brazil) (Fig. 4). La retro-obturación se realizó con Biodentine, preparado según las indicaciones del fabricante (Septodont, Saint Maur de Fossés, France) (Fig. 5), transportado al canal radicular con una espátula de resina y condensado con un microcondensador previo a irrigación por vía retrógrada con Clorhexidina al 2% (Encident clorhexidina, Blenastor ,Quito, Ecuador) aspiración constante y secado con puntas de papel.
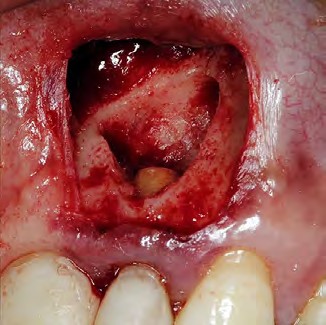
Figura 4. Limpieza del campo quirúrgico y caja de obturación.
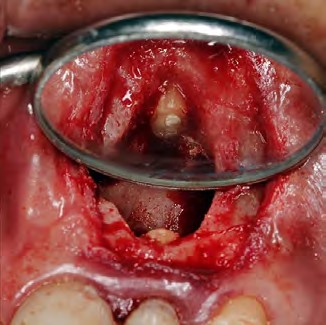
Figura 5. Obturación Retrógrada con Biodentine.
Se lavó la cavidad ósea con solución fisiológica, eliminando el remanente tejido y cemento con el fin de proporcionar una zona libre de contaminación ideal para la colocación del injerto óseo. Se utilizó 1cc de xenoinjerto particulado de origen bovino (InterOss®, SigmaGraft Inc., Fullerton, California, USA) (Fig. 6), éste se colocó en la cavidad ósea y fue cubierto con membrana de colágeno reabsorbible (InterCollagen® Guide,SigmaGraft Inc., Fullerton, California, USA).
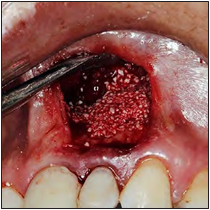
Figura 6. Colocación de Xenoinjerto óseo.
Se procedió a reposicionar el colgajo con sutura Nylon 4-0 (Silkam 4-0, B Braun Medical, Seesatz, Switzerland), con puntos simples (Fig. 7), y finalmente se realizó una radiografía periapical postoperatoria de control. La obturación vía ortógrada (Fig. 8) se realizó con una técnica de compactación lateral con gutapercha (Alfred Betch, Germany) y cemento resinoso AH Plus sealer (Dentsply, De Trey Konstanz, Germany) se completó el mismo día. Finalmente el paciente recibió indicaciones postoperatorias.
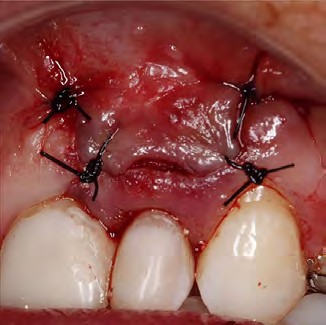
Figura 7. Reposición y sutura del colgajo
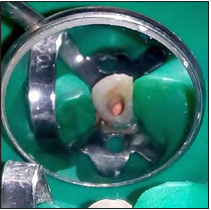
Figura 8. Obturación vía ortógrada.
El control radiográfico fue efectuado a los 6 y 12 meses evidenciando ausencia de zona radiolúcida apical y sin presencia de signos ni síntomas. (Fig. 9)
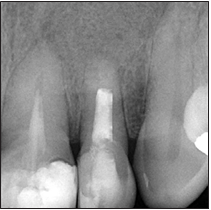
Figura 9. Radiografía de control final.
Discusión
La periodontitis apical es una lesión inflamatoria en los tejidos periradiculares en respuesta a una infección bacteriana intrarradicular. (1) Se ha preconizado que una lesión de más de 1 cm de diámetro, bordes definidos y con línea radiopaca que rodea la lesión puede tener un diagnóstico de quiste 10, sin embargo, otros autores afirman que el estado histológico no puede ser definido por el tamaño de la lesión (11,12). Lesiones pequeñas, grandes, o el ensanchamiento del espacio del ligamento periodontal pueden ser granulomas, abscesos o quistes y se diagnostican con exactitud mediante un examen histopatológico. El tamaño de la radiolucencia dependerá también en gran medida del tiempo de desarrollo de la patología. (11,12) Se debería denominar a estas imágenes radiolúcidas con el término general de periodontitis apical.
Un tratamiento endodóntico ortógrado debería ser suficiente para solucionar un proceso apical, sin embargo, en la práctica clínica la persistencia de infección puede comprometer la tasa de éxito. Se han reportado varios casos de lesiones recalcitrantes al tratamiento otorgado, las cuales contenían un componente extrarradicular de infección bacteriana (2,12), que están relacionadas con el tipo y la virulencia de las bacterias implicadas y la resistencia del huésped. Esta condición puede ser una extensión del proceso infeccioso intrarradicular causado por bacterias que invaden los tejidos perirradiculares, convirtiéndose en una entidad independiente y superando las defensas locales del huésped, dando lugar a síntomas y/o a la formación de una lesión. Si no hay una respuesta favorable al tratamiento convencional, indicaría que deben ser tratadas con altas probabilidades de éxito mediante cirugía periapical. (10,12)
La cirugía periapical antes se basaba en la eliminación de tejido alrededor de la lesión y una porción de raíz, intentando limpiar toda la zona afectada sin dar suficiente importancia al sellado apical. Actualmente, se comprobó que si no existe un sellado apical el hueso no regenera, aunque todo el tejido patológico hubiera sido eliminado; la causa es una persistente comunicación entre el canal radicular y el periodonto (12,13). Se sabe que el éxito de un tratamiento endodóntico quirúrgico o no quirúrgico depende de varios factores, entre ellos que exista un sellado apical que forme una barrera entre el canal radicular y el periodonto. (14,15)
En el presente caso con antecedentes de cirugía y ápice abierto, se considera dos opciones: vía ortógrada se puede realizar apicoformación o vía retrógrada una retroobturación (14,16). El material ideal de sellado para la retroobturación debe mostrar capacidades como ser insoluble en fluidos tisulares, dimensionalmente estable, antibacteriano, conductor de tejido duro, biocompatible, radiopaco, fácil de manejar y no tóxico. (17)
Biodentine (Septodont, Saint Maur de Fossés, France) es un material a base de silicato de calcio, el cual está muy cerca de ser un material ideal, puesto que varios estudios muestran excelentes propiedades de sellado, además de inducir la formación de cemento y la reparación completa del ligamento periodontal. (9,18)
Como lo indican en sus estudios Vipin Arora y Raghavendra S. en el año 2013 y 2017, respectivamente, que durante la fase de fraguado de Biodentine se liberan iones de hidróxido de calcio, dando como resultado un pH alcalino de aproximadamente 12,5, el cual inhibe el crecimiento de microorganismos (19); además genera adhesión micromecánica debido a la disolución de tejido orgánico en la entrada del túbulo donde puede entrar formando conos microscópicos. dando lugar a un anclaje estable y sellado hermético. (19,20)
El uso de antibióticos como primera elección fue descartado, tomando en cuenta la guía de uso de antibióticos sistémicos en endodoncia de la Asociación Americana de Endodoncia (21). Por otro lado, autores como Segura y cols (22) mencionan que los antibióticos sistémicos deberían reservarse para pacientes con Absceso Dentoalveolar Agudo, que presenten síntomas sistémicos, infecciones progresivas, o sean inmunocomprometidos; se contraindica el uso en abscesos apicales crónicos, sin embargo, está aceptado su uso en infecciones persistentes con exudación crónica que no es resuelta por procedimientos y medicación intracanal.
Taschieri y cols mencionan que la regeneración ósea guiada debería realizarse solamente en casos de lesiones bicorticales (23); coincidiendo con Igor Tsesis y cols, que demostraron que tanto en lesiones bicorticales, apicomarginales y en grandes lesiones, el resultado fue favorable cuando se usó sustitutos óseos y/o membranas. (24) El uso de membrana reabsorbible de origen porcino reticulado se basa en el concepto de que las células epiteliales migran aproximadamente diez veces más rápido que otros tipos de células periodontales; éstas se excluyen del espacio de la herida el tiempo suficiente para que se establezcan otros tipos de células, como los osteoblastos con potencial regenerativo y osteoconductor. (24) El xenoinjerto de tejido óseo está preparado de muestras corticales bovinas, se compara químicamente y estructuralmente al de humano mineralizado, dando como resultado partículas fluidas no inmunogénicas que son reemplazados por hueso huésped en 4-24 semanas (25), es decir, que su tasa de sustitución es lenta, de esta forma se mantiene el volumen del tejido durante y después de la regeneración ósea. (26)
Según varios autores, con el uso de magnificación la endodoncia quirúrgica eleva significativamente las tasas de éxito hasta un 80 %, mejora la capacidad de localizar, limpiar y llenar el sistema del canal radicular, logrando así un resultado predecible. (6,7)
Conclusión
Las infecciones extra radiculares son entidades independientes al canal radicular que comprometen el éxito de la endodoncia.
El tamaño de la lesión no decide en ningún caso si la endodoncia será o no quirúrgica; la decisión debe basarse en las circunstancias individuales de cada caso.
El uso de materiales a base de silicato de calcio en conjunto con la magnificación y ultrasonido logran resultados más predecibles en endodoncia quirúgica.
Referencias Bibliográficas
1. Ricucci D, Lopes W, Loghin S, et.al. Large Bacterial Floc Causing an Inde- pendent Extraradicular Infection and Posttreatment Apical Periodontitis: A Case Report. J Endod. 2018 Aug;44(8):1308-1316
2. Ricucci D, Siqueira J, Lopes W. Extraradicular Infection as the Cause of Per- sistent Symptoms: A Case Series. J Endod 2015 Feb;41(2):265-73
3. Baek S, Plenk H, Kim S. Periapical Tissue Responses and Cementum Rege- neration with Amalgam, SuperEBA, and MTA as Root-End Filling Material. J Endod. 2005 Jun;31(6):444-9
4. Faisal A, Abdulrahaman A, Samar A. Healing of Periapical Lesions After Sur- gical Endodontic Retreatment: A Systematic Review. A Systematic Review. Cureus. 2020; 12(2): 69-16
5. Syngcuk Kim, Samuel Kratchman, Garrett Guess. Contemporary Endodon- tic Microsurgery: Procedural Advancements and Treatment Planning Conside- rations. American Association of Endodontists.2010;
6. Taschieri S, Del Fabbro M, Testori T, et. al. Endodontic Surgery Using 2 Diffe- rent Magnification Devices: Preliminary Results of a Randomized Controlled Study. J Oral Maxillofac Surg. 2006 Feb;64(2):235-42.
7. Del Fabbro M, Taschier S. Endodontic therapy using magnification devices: A systematic review. J Dent. 2010 Apr;38(4):269-75.
8. Lin C, Lee C, Chen L, et. Alt. Treatment time for non-surgical endodontic the- rapy with or without a magnifying loupe BMC Oral Health. 2015 Mar 20;15:40.
9. Caron G, Azérad J, Faure M, Machtou P, Boucher Y. Use of a new retrograde filling material (Biodentine) for endodontic surgery: two case reports. Int J Oral Sci. 2014 Dec;6(4):250-3.
10. Eugene Natkin, Robert J. Oswald, Lawrence Carries. The relationship of le- sion size to diagnosis, incidence, and treatment of periapical cysts and granu- lomas. Oral Surg Oral Med Oral Pathol. 1984 Jan;57(1):82-94.
11. Abbot P. Classification, diagnosis and clinical manifestations of apical perio- dontitis. Endodontic Topics. 2004;8: 36–54.
12. Peñarrocha D, Peñarrocha M, Escoda C.Cirugía Periapical Básica. Ed. Uni- versitat de Valencia. 2019.
13. Abusrewil S, McLean W, Scott J. The use of Bioceramics as root-end fi- lling materials in periradicular surgery: A literature review. Dent J. 2018 Oct;30(4):273-282
14. Sonu Gupta, Surender Pal Singh Sodhi, Gursimrat Kaur Brar, Ravinder Nath Bansal. Endodontic treatment of immature tooth: A challenge. Journal of Pre- Clinical and Clinical Research. 2020; 14(3):73-79.
15. Dioguardi M, Di Gioia G, Illuzzi G. Inspection of the Microbiota in Endodon- tic Lesions. Dentistry Journal. 2019;7(47).
16. Bala N, Bhullar K, Sapra M. Surgical management of large periapical lesion using prf and mta: a case report. International Journal of Research in Health and Allied Sciences. 2016; 2(4).
17. Wang Z. Bioceramic materials in endodontics. Endodontic Topics. 2015; 32: 3–30
18. Bani M, Sungurtekin E, Enes M. Efficacy of Biodentine as an Apical Plug in Nonvital Permanent Teeth with Open Apices: An In Vitro Study. Biomed Res Int. 2015;2015:359275.
19. Arora D, Nikhil V, Sharma N, et.Alt. Bioactive dentin replacement. IOSR Journal of Dental and Medical Sciences.2013; 12(4): 51-57.
20. Raghavendra SS, Jadhav GR, Gathani KM, Kotadia P. Bioceramics in en- dodontics - a review. J Istanb Univ Fac Dent. 2017 Dec 2;51(3 Suppl 1):S128- S137.
21. Ashraf F, Chair, B. Ellen A, et al. Cha. AAE Guidance on the Use of Systemic Antibiotics in Endodontics. American Association of Endodontists. 2017.
22. Segura-Egea JJ, Gould K, Şen BH, Jonasson P, Cotti E, Mazzoni A, Sunay H, Tjäderhane L, Dummer PMH. Antibiotics in Endodontics: a review. Int Endod J. 2017 Dec;50(12):1169-1184.
23. Taschieri S, Testori T, Azzola F. Guided tissue regeneration in en- dodontic surgery. Rev Stomatol Chir Maxillofac. 2008; 109:213-217.
24. Corbella S, Taschieri S, Elkabbany A, Fabbro M, Arx T. Guided Tissue Re- generation Using a Barrier Membrane in Endodontic Surgery. SWISS DENTAL JOURNAL SSO. 2016; 126: 13–25.
25. Prasanna J, Karunakar P, Rajashree D, et al. Bone regeneration in a perio- dontally challenged hopeless toot. Journal of Dr. NTR University of Health Sciences. 2013;2(4): 296-30.
26. Serrano C, Castellanos P, Botticelli D. Use of Combination of Allografts and Xenografts for Alveolar Ridge Preservation Procedures: A Clinical and Histolo- gical Case Series. Implant Dent. 2018 Aug;27(4):467-473.







